根拠に基づく新しい認知症ケア「キョウメーションケア(Kyomation Care)」~介護者にとって負担となる種々の症状~
進化は、遺伝子の変化で生じる。もちろん脳の進化も遺伝子によるものです。
脳は進化するにつれ高度な機能や心も進化してきたわけだが、その過程で私たちが生きていくために必要な五感などから入ってくる情報を処理する能力は特別に進化したといえます。つまり、ヒトは進化するにつれて処理する情報が増し、必然的に、対応する脳の部分が局在的に巨大化してきたわけです。
特に言語に関する脳は凄まじい進化を遂げているし、脳幹部が垂直に下を向いているのも先祖が直立二足歩行を始めたからだと考えられているのです。
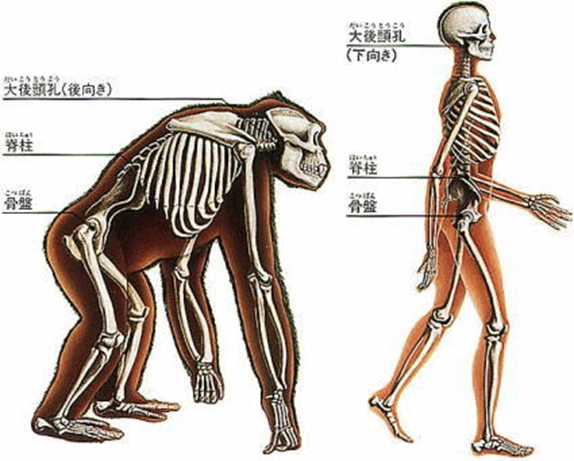 また、大脳の中では進化と共に様々な機能分化が起こり他の動物には無い予測や判断と言った高度な機能、いわゆる「知性」と呼ばれるものを生みだしていったのです。
また、大脳の中では進化と共に様々な機能分化が起こり他の動物には無い予測や判断と言った高度な機能、いわゆる「知性」と呼ばれるものを生みだしていったのです。
知性とは、大脳の6つの連合野で五感や運動の情報を高次元で処理することを指しています。
おもに、前頭連合野は注意、思考、意欲、情動そして短期記憶に関係し、頭頂連合野では触覚や視覚の情報と手足の運動を結びつけて制御しています。
後頭連合野は視覚の情報を高次に分析、総合しているし、側頭連合野は長期記憶に関係するだけでなく、感覚性言語野があり聴覚の情報を分析、処理もしているのです。
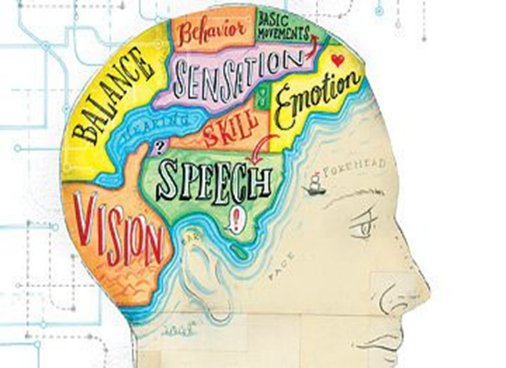 そして、運動連合野は、ある決められた運動プログラムを作り、それを運動野に伝える働きを行い体性連合野は、体が受ける複雑で機械的な刺激を処理しているのです。
そして、運動連合野は、ある決められた運動プログラムを作り、それを運動野に伝える働きを行い体性連合野は、体が受ける複雑で機械的な刺激を処理しているのです。
また、知性を補う性格に関しては、素質は遺伝的に、形成は環境による影響が大きいといわれ、この性格こそが認知症ケアの最大の難問となっているのです。
このように連合野で機能の低下や障害が起きると進行性の中核症状だけでなく随伴して周囲の状況や環境が解釈できなくなるなどの混乱をきたします。
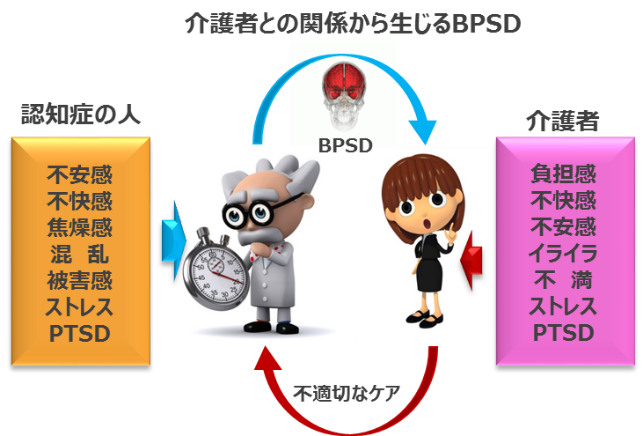
これを、認知症の行動・心理症状(Behavioral and Psychological Symptoms of Dementia:BPSD)と呼んでいます。
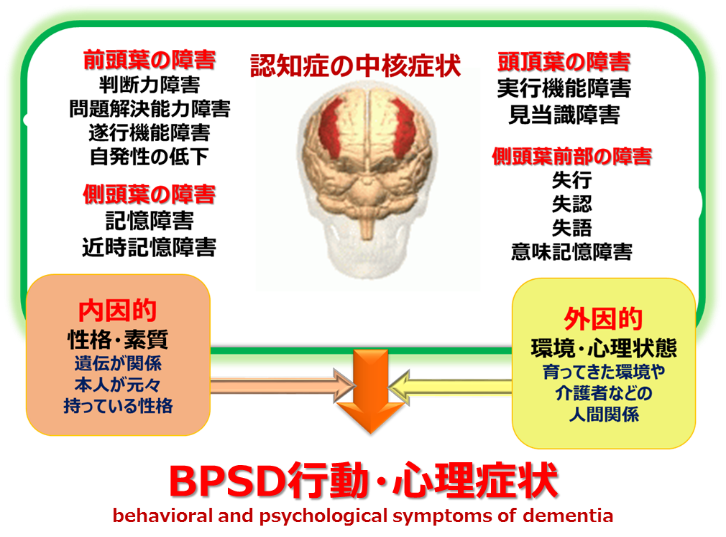 BPSDには多数の原因があり、内因的なものには遺伝的なものとの関連があり、外因的なものには後天的な環境の変化や介護者の要因が重大な関わりを持っているといわれています。
BPSDには多数の原因があり、内因的なものには遺伝的なものとの関連があり、外因的なものには後天的な環境の変化や介護者の要因が重大な関わりを持っているといわれています。
認知症の介護を行っていくためには、認知症の人が示す様々な症状を理解しなければなりません。その実態を知らない限り、ただただ理解不能な得体のしれない現象としか見えないからです。
実は、1980年代は、このような高度な物忘れや不可解な混乱状態などの症状を問題行動と呼んでいたのですが、その後、1999年16カ国から専門家が60名ほど参加したコンセンサス会議に於いて、問題行動という用語の代わりに認知症の行動・心理症状BPSDと呼び、認知症の人に頻繁に見られる知覚、思考内容、気分または行動の障害による症状と定義したのです。(Finkel and Burns, 1999)
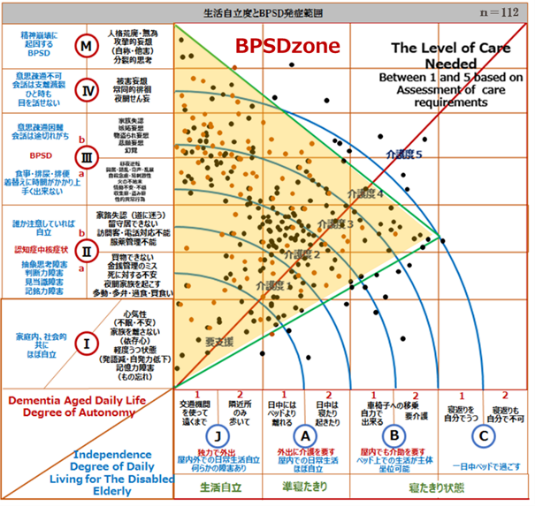 行動症状とは、通常は認知症の人の観察によって明らかにされる攻撃的行動、叫声、不穏、焦燥、徘徊、文化的に不釣り合いな行動、性的脱抑制、収集癖、ののしり、つきまといなどであり、右図の黒点部で多く観察されています。
行動症状とは、通常は認知症の人の観察によって明らかにされる攻撃的行動、叫声、不穏、焦燥、徘徊、文化的に不釣り合いな行動、性的脱抑制、収集癖、ののしり、つきまといなどであり、右図の黒点部で多く観察されています。
心理症状とは、本人や家族との面接によって明らかにされる不安、抑うつ、幻覚、妄想などで、赤点部で多く認められています。
このような症状は認知症の進行過程の一部として避けられないため、本人だけでなく家族や介護者のストレスや介護費用の増大を伴うなど深刻な問題をもたらしているのです。
BPSDの原因解明を考えてみると、4つの要因が組み合わされていることに気づかされます。
それは、外界の刺激を情報に変換する受容体と呼ばれるレセプターが遺伝的に障害される遺伝的要因、神経伝達物質の低下や現象による要因、性格やストレスなど心理学的要因、そして、環境や人間関係などの社会的要因です。
しかし、それらの要因が関わる程度は、個々の症状ごとに異なり大雑把な関係しか見いだせておらず、明確な結論を得るには至っていないのです。
 2015年3月に発表された画期的な新薬と言われる「抗アミロイドβ(Aβ)抗体」においても、今のところ効果が示されたデータは過去15年間の臨床試験に於いて無いと言われています。
2015年3月に発表された画期的な新薬と言われる「抗アミロイドβ(Aβ)抗体」においても、今のところ効果が示されたデータは過去15年間の臨床試験に於いて無いと言われています。
これは発症期には、既に脳の萎縮が始まってしまっているからだと言えます。
マウントサイナイ医科大学の塩井純一博士によると本当にこれらの抗体が有効かどうかは、今後20年は待たないと難しいと言います。
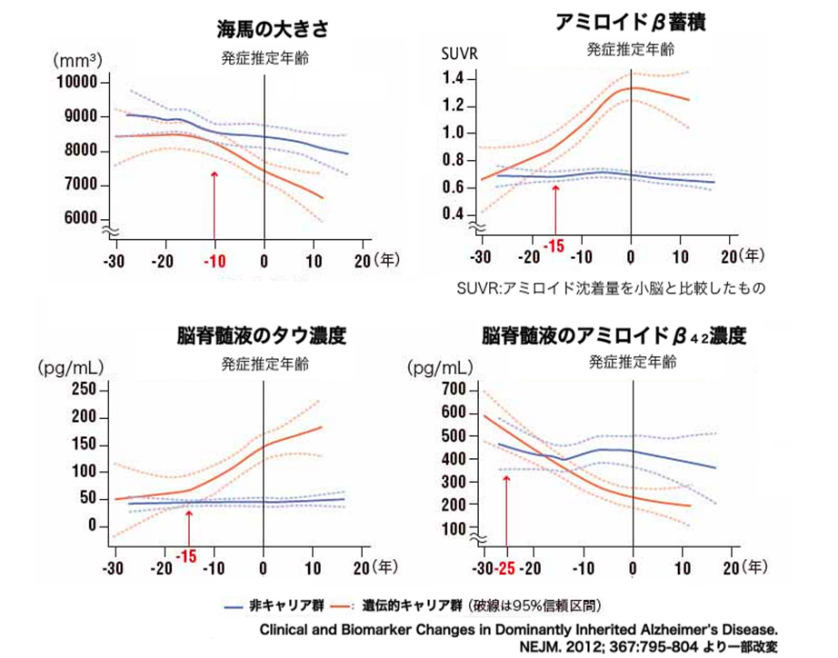 アミロイドの沈着はアルツハイマー病の発症20年前に始まっているのですから、発症時期が判っているFAD(familial Alzheimer’s disease)突然変異の保持者を対象に発症予定年齢の20年前に治療してから20年後発症しない事を確認しなければならないからです。
アミロイドの沈着はアルツハイマー病の発症20年前に始まっているのですから、発症時期が判っているFAD(familial Alzheimer’s disease)突然変異の保持者を対象に発症予定年齢の20年前に治療してから20年後発症しない事を確認しなければならないからです。
また、FAD突然変異をもつ患者はアルツハイマー病全体の1%以下にすぎないので、逆に被験者を集める方が大変になると言えます。
一方、アルツハイマー病の危険因子であるアポe4保持者を対象に発症前の試験的治療が始まっているのですが、必ず発症するか不確定なので、統計的な有意差を得るためには膨大な数の被験者(数万人のビッグデータ)を必要とするので、これは科学的に信頼できるデータを得るのが難しいと考えられています。
依然アミロイド仮説に基づく治療の可能性はあると思いますが、発症期の短期間の治療で有効か、はたまた10年20年に及ぶ長期治療が必要かも判らず、長期服用の場合の副作用の検証も考えると今後30年~50年は必要になるでしょう。
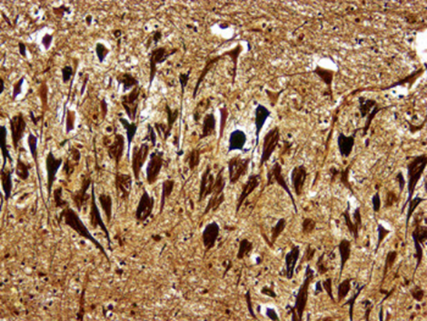 最近のPET scanによりNFT(Neurofibrillary tangles)神経原線維変化は発症前の数年から10年前後と判って来ており、これの出現と神経細胞死がかなり密接な関係なので、NFTの構成分子であるリン酸化タウを標的とした治療法の開発はかなり短く済む可能性があります。それでも10年~20年はかかるのではないでしょうか。
最近のPET scanによりNFT(Neurofibrillary tangles)神経原線維変化は発症前の数年から10年前後と判って来ており、これの出現と神経細胞死がかなり密接な関係なので、NFTの構成分子であるリン酸化タウを標的とした治療法の開発はかなり短く済む可能性があります。それでも10年~20年はかかるのではないでしょうか。
残念ながら現時点では、認知症に対する薬物の果たす役割はそれほど目覚ましいものではないため、薬物を用いない対症療法ともいえる介護の役割が極めて大きくなるわけです。
まず、4つの要因のうち遺伝的要因との関連を見てみると、アルツハイマー型認知症における精神病症状の出現などは、精神病の家族との関連性が高いことが分かっているし、ドパミン受容体と精神病との関連性も認められているのです。
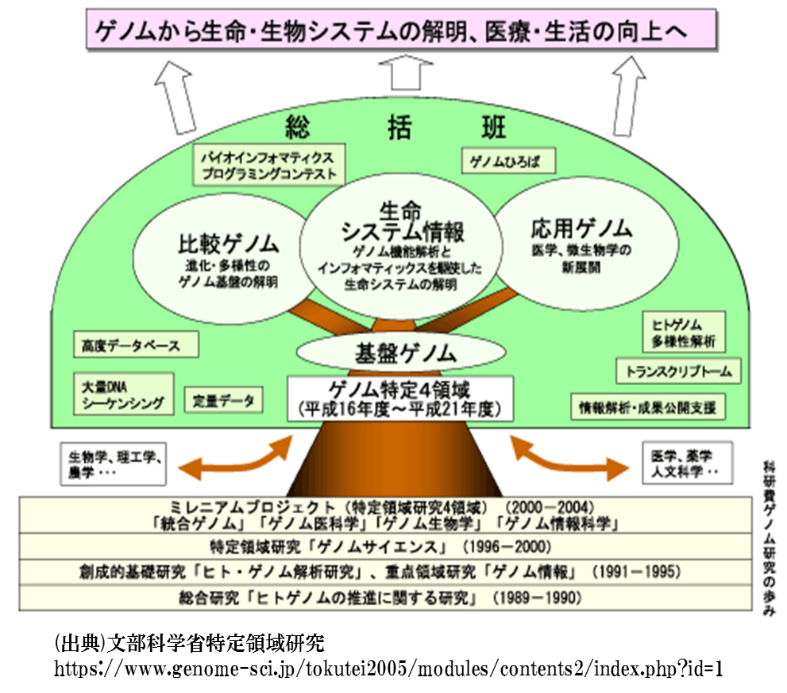 1953年ワトソンとクリックによって遺伝子のもとになるDNAモデルが提唱され、2003年にはDNAの配列であるゲノムの構造が解明されたことは認知症の本格的なゲノム研究に突入する端緒となりました。
1953年ワトソンとクリックによって遺伝子のもとになるDNAモデルが提唱され、2003年にはDNAの配列であるゲノムの構造が解明されたことは認知症の本格的なゲノム研究に突入する端緒となりました。
そして、その後のゲノム研究によって人の性格は親に似ていたり、行動や能力が遺伝の影響を受けるなど、行動や心理には遺伝的要因が多く関与していることがわかってきたのです。
例えば、神経伝達物質セロトニンを再取り込みするセロトニントランスポーター遺伝子は統合失調症のリスクを増大させているし、「やる気」は、脳内で分泌されるドパミンによって支配されており、そのドパミンの分泌には特定の遺伝子がかかわっている。
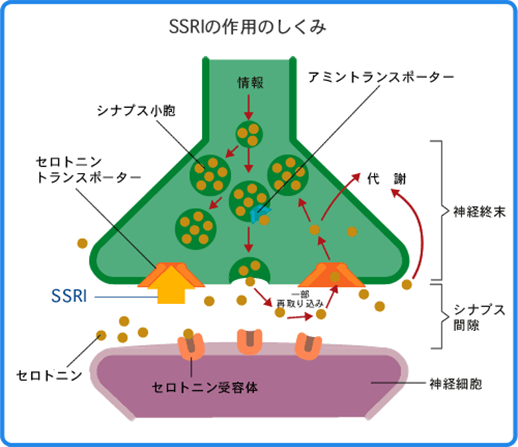 トリプトファン遺伝子は攻撃性に、ドパミンD1遺伝子は焦燥感にドパミントランスポータ遺伝子は常軌を逸した運動行動および易刺激性に関連していることが見出されている。また、妄想や攻撃性はapoE4遺伝子が関連しているなど遺伝子的異常と個々のBPSDの症状との相関に関する知識を高めることは、BPSDの対症療法やケアの工夫には有用と言えるのではないでしょうか。
トリプトファン遺伝子は攻撃性に、ドパミンD1遺伝子は焦燥感にドパミントランスポータ遺伝子は常軌を逸した運動行動および易刺激性に関連していることが見出されている。また、妄想や攻撃性はapoE4遺伝子が関連しているなど遺伝子的異常と個々のBPSDの症状との相関に関する知識を高めることは、BPSDの対症療法やケアの工夫には有用と言えるのではないでしょうか。
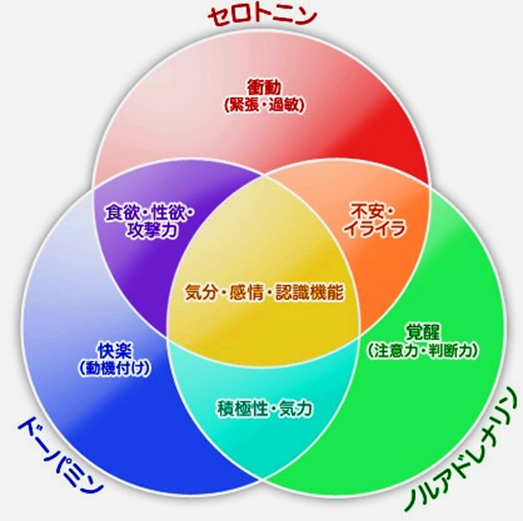
キョウメーションケアでは、BPSDの出現にはセロトニンを多く分泌する遺伝子を持つと「他人との結びつきを求め」「幸福感」を感じやすく多幸になる傾向がみられ、一方、セロトニンが減ると「不安」になり「うつ病」の原因になるなど、セロトニンの重要性が際立っていると考えています。
BPSDとは、本人の心に深く刻まれた過去の経験の記憶に支配された行動なのかもしれませんね。
最近の認知症研究は、行動・心理症状BPSDの出現や進行を遅らせることに重点が置かれている。そのための新薬の臨床試験もアルツハイマー病を引き起こす遺伝子変異を持つ人々を対象に始まっています。
レセプター遺伝子変異を持つ3種類の遺伝子、例えばプレセニン(presenilin)なども見つかったのですが、このような遺伝子変異が原因の症例は全体の数パーセントに過ぎない、むしろ加齢の影響から神経細胞を守るREST(repressor element1-silencing transcription factor)別名NRSFと呼ばれるタンパク質が減少すると中核症状が発症し、BPSDが出現してくると最近の研究では考えられているのです。
 このように神経伝達物質の低下をはじめ性格やストレス、そして環境の変化や人間関係などが組み合わされることが極めて影響しているわけです。
このように神経伝達物質の低下をはじめ性格やストレス、そして環境の変化や人間関係などが組み合わされることが極めて影響しているわけです。
脳の機能は、高次になればなるほど複雑になることは脳の進化で述べましたが、同じ刺激に対しても人それぞれ対応が違うことになります。これが性格と関係して様々なストレスを生む要因になっていると考えられており、脳もまた、認知機能の障害が困惑と混乱で酷使されると、いわゆるストレスがたまった状態になりBPSDが出現するのかもしれません。
例えば、本人が何か意味不明なことを言い出した時に、そうではないと説得したり、そんなことはしてはだめですよと反ばくしたりして、論争になることで本人の心がとがめられて不愉快だったという感情が残ってしまいます。
それだけでなく説得しようとしたり否定したりすると、かえって混乱して、ストレスから一層BPSDがひどくなってしまうのです。
 BPSDは局在的な脳の病巣に由来して現れることや様々な認知症の疾患によってパターンも異なることもいわれている。
BPSDは局在的な脳の病巣に由来して現れることや様々な認知症の疾患によってパターンも異なることもいわれている。
心のストレスは計りにくいものである。
本来ストレスとは、ある刺激に対してどう受け止めたか、どう反応したかということを指す。だから、「楽しい」と感じる快感も「つらい」「苦しい」と感じる不快感もストレスなのです。ただ、不快感ばかりが長く続くとBPSDの引き金となるということです。
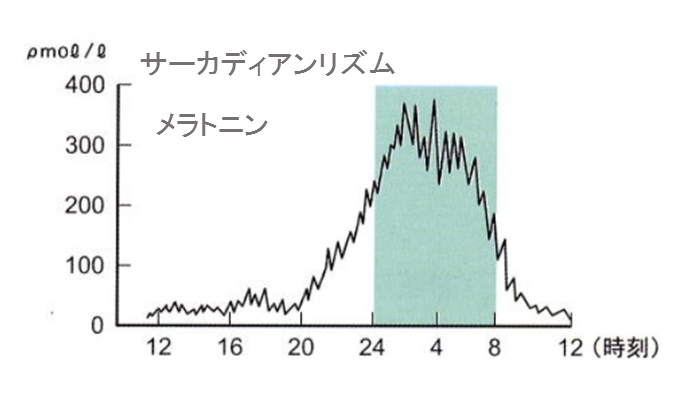
その一つが、サーカディアン・リズム障害と呼ばれる概日リズムが乱れてBPSDが生じることです。
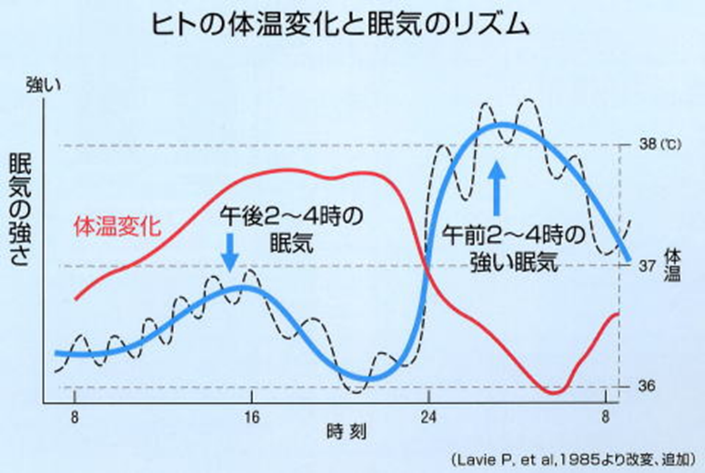 これは、認知症により睡眠パターンに異常が起こり、日常生活を営むために必要な睡眠パターンとの間に生体現象のズレを生じさせて日中は焦燥と傾眠、夜間は不穏という症状をもたらしてしまうのだ。さらに概日リズムの異常は「夕暮症候群」の原因になることもあるのです。
これは、認知症により睡眠パターンに異常が起こり、日常生活を営むために必要な睡眠パターンとの間に生体現象のズレを生じさせて日中は焦燥と傾眠、夜間は不穏という症状をもたらしてしまうのだ。さらに概日リズムの異常は「夕暮症候群」の原因になることもあるのです。
キョウメーションケアでは、多くの場合、社会的役割の喪失や環境の変化など生活上の出来事の後や、あるいは身体的不快感や疾患が進行するとBPSDを出現すると予測しています。
 しかし、高次脳機能のすべてが障害されて発症しているのではなく、ストレス要因と原因脳病変によって失われていく機能と、原因脳病変が及ばず失われずに保たれる機能とがあるということも念頭に入れておくことが認知症ケアには重要と考えています。
しかし、高次脳機能のすべてが障害されて発症しているのではなく、ストレス要因と原因脳病変によって失われていく機能と、原因脳病変が及ばず失われずに保たれる機能とがあるということも念頭に入れておくことが認知症ケアには重要と考えています。
また、遺伝的要因に随伴して認知症を発症した人の脳では、神経生物学的要因と言われる複数の神経伝達物質の変化が認められています。
アセチルコリンの濃度の低下は記憶障害、混乱、せん妄を引き起こします。
せん妄では、幻覚や妄想、睡眠の断片化や足で床を叩いたり、手を揉んだりする精神運動性興奮を伴います。
ドパミンの濃度低下などは作業記憶などの認知機能に関わって攻撃性および焦燥と関連しています。しかし、そうした変化とBPSDとの間には大雑把な関係しか見いだせておらず、残念ながら現時点でのBPSDに対する治療は、すべて対処療法であり現在使われている薬剤からは望むべくもないのです。
したがって、BPSDにおいては、薬物を用いない対症療法ともいえるケアの役割が極めて大きく治療の可能を秘めており、認知機能障害に比べると苦悩を和らげたりすることもできるのです。
また、BPSDでも泣き叫び、ののしる、無気力、繰り返し尋ねる、つきまとうなどは、本人の生活史をよく理解している介護者が側にいて関わることで軽減もしくは緩和も出来ています。焦燥、不適切な行動、性的脱抑制、部屋の内外を行き来する、叫声などは介護を困難にさせるのですが必ず何かきっかけがあるはずだと考えて、丹念に本人の話を傾聴して観察すれば、不適切な行動は何かが気に入らないのだから、何が気に入らないのかを見つけることで適切にケアが行へ緩和することも出来ます。
しかし、攻撃的行動、徘徊、不穏などは脳機能障害に基づく病態として、正確に理解し、それに対する理屈にあった科学的な対策のケアを行わなければなりません。
このような場合は様子を観察し原因を見出し、その原因を解消するように説得したり否定するのではなく、保たれている機能を活用して失われた機能を補っていくように「これをしてみませんか」「一緒にこれをやりませんか」などと日常生活動作を利用した自立支援を中心に勧めると落ち着いてくることが少なくありません。
また、症状を抑える薬を止むを得ず使わざるを得ない場合には、誰が、いつ、どのようになど薬を管理する体制もしっかりと行うことが大切です。
妄想、誤認、幻覚、抑うつ、不眠、不安などの心理症状は照度や気圧など気象の変化だけでも頻回に出現する極めて厄介で対処が難しいBPSDです。
このような症状をケアするためには、本人をよく知っている介護者が辛抱強く観察と、こういう症状の時には、こうしたらうまくいったとか、こうしたら失敗したというような記録を積み重ねて、それに基づいて介護者がケアを工夫したやり方を試みることです。
また、身体疾患や合併症、薬物もBPSDの原因になるので確認しておくとよいでしょう。